8月22日,由迈迪思创作为战略赋能伙伴全程辅导申报的“一次性无菌微结构硅胶导尿管”,经陕西省药品监督管理局依据《陕西省第二类创新医疗器械特别审查许可程序(试行)》正式获批,成为陕西省首个获认定的二类无源创新医疗器械。该产品的成功认定,不仅实现了省内该类产品创新审查“零的突破”,也为创新路径下其他无源产品的申报提供了重要实践范本。
一、项目背景与创新价值
陕西善洁沐恩生物技术有限公司引进美国Sharklet技术,推出表面具有鲨纹微结构的硅胶导尿管,该产品通过物理方式抑制细菌定植与迁移,无需化学涂层,即可实现抑制细菌再生、进而降低患者痛感的临床功效。
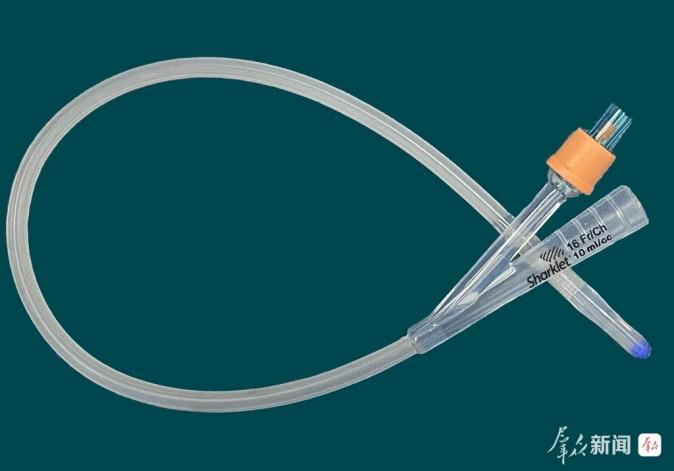
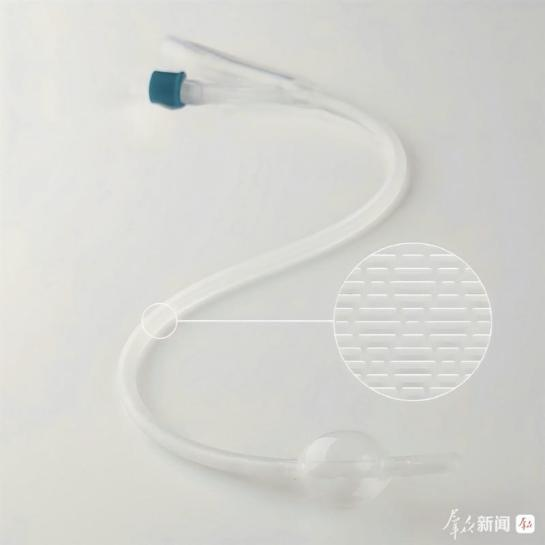
(图片来源:陕西日报数字报-群众新闻网)
其创新价值体现在:
• 技术原创:采用微米级拓扑结构设计,通过表面能降低、接触面积减少和毛细作用抑制等机制,阻断生物膜形成路径;
• 标准引领:牵头制定ASTM E3285-22国际标准及中国团体标准T/EDSA 002-2019,获中美双认证;
• 临床验证:经GLP合规检验及欧洲临床试验(NCT02835456),证实可显著减少生物膜面积并降低患者疼痛感。
二、 回溯:应对三大审查程序的核心挑战与解决方案
本次创新申报必须严格符合《陕西省第二类创新医疗器械特别审查许可程序(试行)》的三项审查程序。迈迪思创作为申报辅导方,核心工作即是针对每项程序要求,提供专业的解决方案,回复和解决审评关注要点:
审查程序一:依法拥有产品核心技术发明专利权,核心技术方案具备新颖性和创造性。
核心挑战:证明“鲨纹微结构”这一物理结构创新不属于常规工艺改进,而是具备专利保护和技术创造性的实质性创新。
解决方案:
• 【证明技术的原创性与合法性】
确立以发明专利“一种表面具有鲨纹微结构的导尿管管体的制造方法”作为核心知识产权,证明技术的原创性与合法性。
• 【证明其技术先进性和行业认可度】
提供该技术牵头制定ASTM E3285-22国际标准及参与制定中国团体标准T/EDSA 002-2019的证明材料,用“标准引领”支持其技术先进性和行业认可度。
• 【证明技术的新颖性】
提供官方检索结果,证实国内无同类“微结构”导尿管产品获批,证明其新颖性。
审查程序二:列入市级以上政府部门重点发展、支持产品项目,解决“卡脖子”技术难题。
核心挑战:如何充分证明该项目属于政府支持且致力于解决“卡脖子”技术问题。
解决方案:
• 【系统梳理政策依据与项目契合度】
深入研究省、市各级相关政策,系统梳理了该项目与政府重点支持方向的高度契合性,从政策层面夯实申报基础。
审查程序三:产品技术国内领先,可填补本省该品种医疗器械的空白或解决临床急需。
核心挑战:提供完整证据链,证明该产品技术领先、填补空白,且其通过表面微结构带来的临床应用价值是真实、迫切的。
解决方案:
• 【证明技术的先进性】
系统梳理了由美国NIH、海军研究办公室等机构支持的前期基础研究数据,证明其技术根源的先进性与国际认可度。
• 【临床价值验证】
提交了共169页的GLP合规检验报告,证实产品能有效抑制七大致病微生物的定植与迁移。
提交了在同源技术的产品在欧洲完成的临床试验报告(NCT02835456),用临床数据证实其“显著减少生物膜”和“减轻患者疼痛”的两大核心临床价值。
• 【本省空白论证】
提供在国家药监局数据库的检索证明,确认“鲨纹”、“微结构”导尿管在陕西省乃至全国均无注册先例,成功证明其“填补空白”的地位。
三、项目成果与行业意义
本次成功认定带来多方价值:
对企业 | 对行业 | 对产业 |
获得创新认定后,产品进入优先检验、审评及审批通道,显著缩短上市周期。企业已计划在西安投资建设研发与智能制造基地,全面投产后预计可实现年产值9.54亿元人民币,进一步增强市场信心与企业的持续投入意愿。 | 实现陕西省二类无源医疗器械创新“零的突破”,为同类产品申报树立标杆,填补技术审评空白,也为物理结构抗菌这一新兴技术路线在医疗器械中的应用提供了审评实践与法规参考。 | 积极响应国家药监局2025年第63号公告中“强化标准引领创新”的倡议,彰显了国际技术合作与中国标准“走出去”的战略价值,为产业高质量发展注入新动能。 |
结语
迈迪思创作为该项目的战略合作伙伴,深度参与了:
从创新性研判、申报策略规划到全程资料编制与沟通协调的全过程。
我们深知,二类创新医疗器械申报常面临诸多难点:
• 如何精准界定创新属性,证明产品并非简单改进
• 如何合理构建临床证据链,提供从实验室到临床的完整数据支撑
• 如何高效对接审评要求,规避因资料不全面或策略偏差导致的失败风险
每一个环节都关乎项目成败,需要前瞻的思考与专业的执行。
若您的产品具有创新潜力,正在筹划申报路径
欢迎联系迈迪思创CRO。
我们将依托丰富经验与专业能力,为您提供定制化解决方案,
共同推动创新医疗技术早日惠及临床。
