对于已经在国际临床广泛应用的成熟医疗器械,如何通过可行的临床评价策略进入中国市场,填补临床空白,已成为企业布局全球战略的重要环节。科学的本土化临床评价策略,正是打通这类产品上市路径的核心利器。
本期“思创者说”将分享迈迪思创作为临床评价与注册赋能伙伴,助力Atos Medical AB(欧拓适)“普罗适(Provox®)”辅助发音管在中国完成临床评价并成功获批的案例。该产品致力于为喉癌术后患者重建发声功能,其获批不仅使国内患者能够同步受益于全球领先的康复技术,也是我们积极响应国家医保局《耳鼻喉科医疗服务价格项目立项指南(试行)》的具体践行——该指南明确提出鼓励开展“发音装置安装/更换”服务,旨在帮助更多患者恢复语音表达能力,更好适应正常的社交生活。
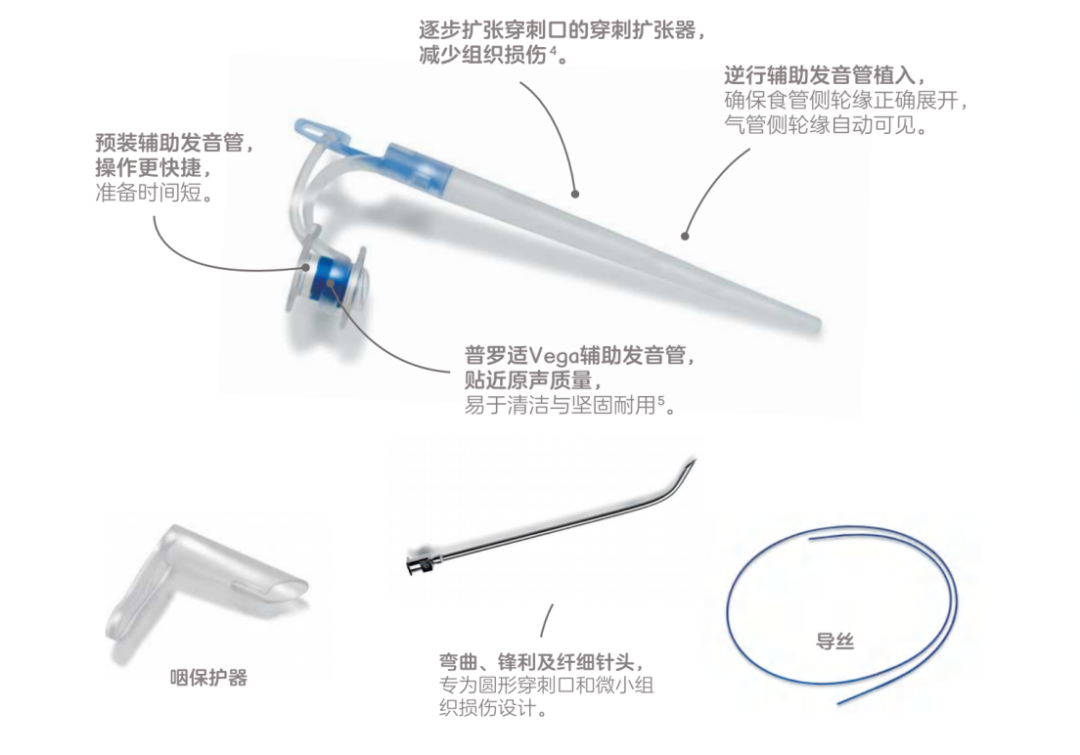
图片来源:Atos Medical AB(欧拓适)官方资料
本案核心价值在于:
我们为这类在国际上已经成熟应用,但在国内尚属空白的产品,设计并成功实践了一条免于境内临床试验的临床评价路径,为其顺利打开中国市场大门提供了关键性的策略支持。
一、项目背景与价值
项目背景:应对喉癌术后言语功能恢复的临床需求
喉癌是头颈部常见恶性肿瘤,部分患者需接受喉全切除术。根据《喉全切除术后辅助发音管植入专家共识(2024版)》,该手术在控制病情的同时会导致患者丧失发声能力,严重影响生存质量与社会参与度。辅助发音管植入是目前国际公认的恢复言语功能的重要方式,在欧美国家已成为临床常规选择,但在我国仍处于推广应用阶段。
政策引领:国家医保局推动发音重建服务体系建设
2025年3月,国家医保局印发《耳鼻喉科医疗服务价格项目立项指南(试行)》,明确提出"帮助更多患者'听得见、说得出'",并专门设立"发音装置安装、发音装置取出/更换"价格项目。该指南从国家层面明确了发音重建服务的临床价值与政策定位,为相关创新技术的应用推广提供了明确的支付政策支持。
二、核心策略回溯:双路径临床评价策略,破解“临床空白”难题
本项目采用双重临床评价路径。鉴于该类产品在中国市场近乎空白,可供选择的比对器械极为有限,本次临床评价创新性地以境内已获批的唯一一款同技术原理产品作为同品种器械参照。通过构建“境外临床数据+境内唯一同品种比对”的双路径论证体系,在免于境内临床试验的情况下,依然形成了完整的证据链,充分证明了申报产品的安全性与有效性:
【境外临床试验数据路径的承接与落地】
我们重点对Atos Medical所提供的境外临床试验资料进行合规性审核与体系化整合,确保其完全符合《接受医疗器械境外临床试验数据技术指导原则》要求。关键工作包括:
系统梳理并提交包括伦理意见、临床试验方案、临床报告在内的完整境外临床试验资料;
重点论证产品在欧盟、美国等成熟市场长期应用的安全有效性数据与中国患者群体的相关性,为其数据被监管部门采信奠定基础。
【同品种比对路径的本地化策略设计与实施】
我们主导完成本土化比对策略的设计与证据组织,为核心论证提供支撑:
精准选择已经在中国获准上市的同类产品作为比对器械,确立比对逻辑;
系统性完成37篇中外临床文献的检索、筛选与综述,重点纳入12篇中国人群临床数据,有力证明产品技术特征和临床获益在中国人群的可移植性;
组织并撰写全面而清晰的等同性论证报告,证明申报产品与比对器械在基本原理、性能参数及适用范围上的高度一致性。
【差异性分析及风险论证】
针对申报产品与比对器械之间的差异,我们系统组织多项证据进行合理解释与支撑:
调用申报产品自身境外数据、前代产品临床文献及全球不良事件监测数据(如MAUDE数据库),证明差异不对安全有效性产生不利的影响;
通过中国境内同品种器械无相关投诉及不良事件的客观事实,佐证该类产品技术成熟、风险可控。
【全程风险管控与证据输出】
我们协助企业进行全球安全性数据监测与趋势分析:
全面检索并分析美国MAUDE、德国BfArM等全球监管数据库中的不良事件与投诉数据,对其中1例死亡事件等严重案例进行归因分析与资料准备;
最终输出清晰、可靠、完整的安全性结论,为产品在中国上市提供关键性风险证据支持。
三、项目成果与意义
临床价值 | 技术价值 | 政策价值 |
通过《专家共识》与医保政策的双重支持,辅助发音管技术有望提升临床应用可及性,为更多喉癌术后患者提供发声功能重建方案。 | 项目展示了在海外成熟应用的进口产品,基于科学的临床评价路径也能在中国注册的可行性,为类似产品提供了注册实践参考。 | 项目实践表明,医疗器械注册工作需密切关注国家医保政策导向,实现产品合规上市与临床可及性的统一。 |
结语
本项目通过创新性的临床评价策略,采用境外临床试验数据与同品种比对相结合的方式,完成了辅助发音管产品的临床证据体系建设。这种评价模式为成熟国际产品进入中国市场提供了科学可靠的注册路径。
若您的产品已在国际市场广泛应用,却对进入中国市场的临床评价路径存在疑虑,欢迎联系迈迪思创CRO。我们依托丰富的国际产品本土化注册经验,为您提供从策略制定到申报的全流程合规解决方案,助力您的产品高效获批,快速惠及中国患者。
